1.6 El carbono en la naturaleza

Propiedades físicas: puede enlazarse con otros átomos de carbono y otros elementos o sustancias para formar miles de compuestos.
Existen cinco formas diferentes en las que se puede encontrar el carbono en la naturaleza:
1. Diamante
-
Estructura: Cada átomo de carbono está unido a 4 átomos más en forma de red tridimensional.
-
Propiedades: Muy duro, transparente, aislante eléctrico, excelente conductor del calor.
-
Usos: Joyas, herramientas de corte y pulido, aplicaciones industriales.
2. Grafito
-
Estructura: El carbono se organiza en capas planas de átomos formando hexágonos. Las capas se deslizan entre sí.
-
Propiedades: Suave, negro, conductor eléctrico, resbaladizo.
-
Usos: Lápices, lubricantes, electrodos, baterías.
3. Carbono amorfo
-
Estructura: No tiene un orden fijo; mezcla de carbono tipo grafito y diamante sin forma definida.
-
Propiedades: Opuestas según la mezcla: puede ser duro o blando, opaco y poco conductor.
-
Ejemplos: Carbón vegetal, hollín, carbón activado.
-
Usos: Filtros, tintas, pigmentos, materiales absorbentes.
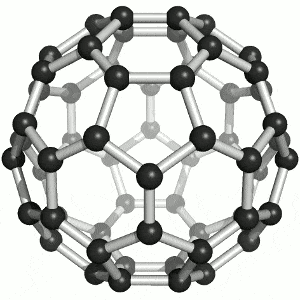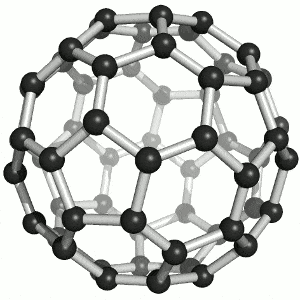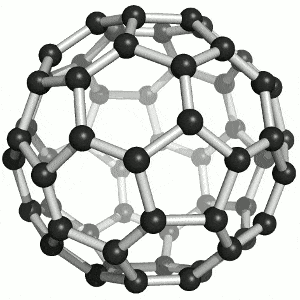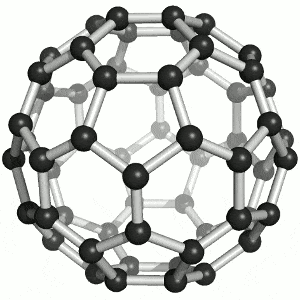
4. Fullerenos
-
Estructura: Átomos de carbono formando esferas, elipsoides o tubos cerrados. El más famoso es C₆₀ (forma de balón de fútbol).
-
Propiedades: Muy estables, ligeros, buena conductividad, capacidad para encapsular otras moléculas.
-
Usos: Nanomedicina, electrónica, materiales avanzados, antioxidantes.
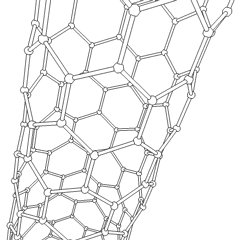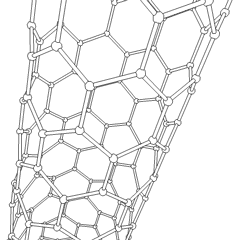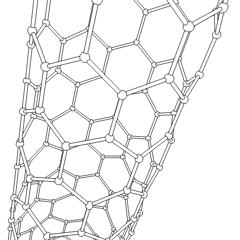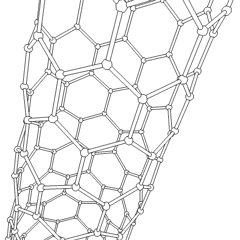
5. Nanotubos de carbono
-
Estructura: Hojas de grafito enrolladas en forma de tubo. Pueden ser de una capa o varias capas .
-
Propiedades: Extremadamente resistentes, excelentes conductores eléctricos y térmicos, muy ligeros.
-
Usos: Nanotecnología, sensores, baterías, materiales ultrafuertes, electrónica.